Kit de diagnóstico para troponina T cardíaca Kit de prueba rápida
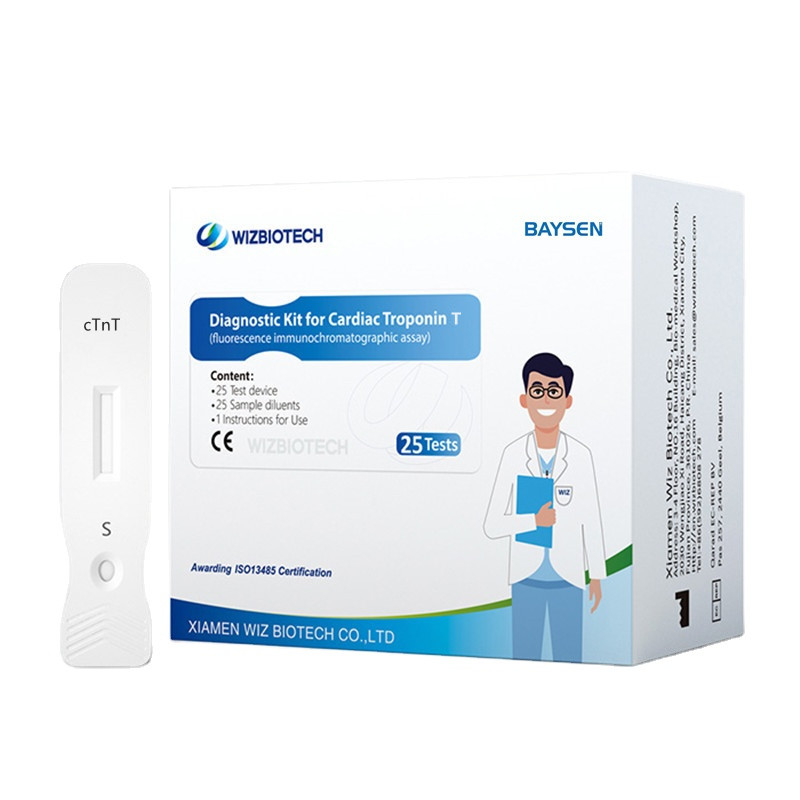
Kit de diagnóstico para troponina T cardíaca
Metodología: Ensayo inmunocromatográfico de fluorescencia
Información de producción
| Número de modelo | cTnT | Embalaje | 25 pruebas/kit, 30 kits/caja |
| Nombre | Kit de diagnóstico para troponina T cardíaca | Clasificación de instrumentos | Clase II |
| Características | Alta sensibilidad, fácil operación. | Certificado | CE/ISO13485 |
| Exactitud | > 99% | Duración | Dos años |
| Metodología | Ensayo inmunocromatográfico de fluorescencia | Servicio OEM/ODM | Disponible |
USO PREVISTO
Este kit está diseñado para la detección cuantitativa in vitro del contenido de troponina cardíaca T (cTnT) en muestras de suero, plasma o sangre completa humanas, y está destinado al diagnóstico auxiliar del infarto agudo de miocardio. Este kit solo proporciona el resultado de la prueba de troponina cardíaca T (cTnT), que debe analizarse junto con otra información clínica.
Procedimiento de prueba
| 1 | Antes de utilizar el reactivo, lea atentamente el prospecto del paquete y familiarícese con los procedimientos de operación. |
| 2 | Seleccione el modo de prueba estándar del analizador inmunológico portátil WIZ-A101 |
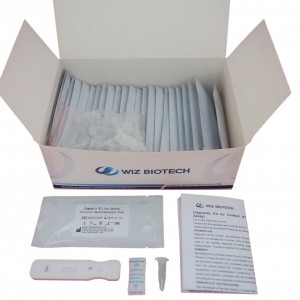
| 3 | Abra el paquete de reactivo envuelto en papel de aluminio y saque el dispositivo de prueba. |
| 4 | Inserte horizontalmente el dispositivo de prueba en la ranura del analizador inmunológico. |
| 5 | En la página de inicio de la interfaz de operación del analizador inmunológico, haga clic en “Estándar” para ingresar a la interfaz de prueba. |
| 6 | Haga clic en “QC Scan” para escanear el código QR en el lado interior del kit; ingrese los parámetros relacionados con el kit en el instrumento y seleccione el tipo de muestra. Nota: Cada número de lote del kit se escaneará una sola vez. Si ya se ha escaneado el número de lote, omita este paso. |
| 7 | Verifique la coherencia del “Nombre del producto”, “Número de lote”, etc. en la interfaz de prueba con la información de la etiqueta del kit. |
| 8 | Saque el diluyente de muestra según la información consistente, agregue 80 μL de muestra de suero/plasma/sangre completa y mézclelos completamente; |
| 9 | Agregue 80 µL de la solución completamente mezclada antes mencionada en el pocillo del dispositivo de prueba; |
| 10 | Después de agregar completamente la muestra, haga clic en “Tiempo” y el tiempo de prueba restante se mostrará automáticamente en la interfaz. |
| 11 | El analizador inmunológico completará automáticamente la prueba y el análisis cuando se alcance el tiempo de prueba. |
| 12 | Una vez completada la prueba con el analizador inmunológico, el resultado de la prueba se mostrará en la interfaz de prueba o se podrá ver a través de “Historial” en la página de inicio de la interfaz de operación. |
Nota: cada muestra deberá pipetearse con una pipeta desechable limpia para evitar la contaminación cruzada.
Superioridad
Tiempo de prueba: 10-15 minutos
Almacenamiento: 2-30 °C/36-86 °F
Metodología: Ensayo inmunocromatográfico de fluorescencia
Característica:
• Alta sensibilidad
• lectura del resultado en 15 minutos
• Fácil operación
• 3 pruebas en una sola vez, ahorrando tiempo.
• Alta precisión

El desempeño clínico
El rendimiento de la evaluación clínica del producto se evalúa mediante la recopilación150Muestras clínicas. Utilice un kit ECLIA comercializado correspondiente como reactivo de control y compare los resultados de la prueba. Utilice la regresión lineal para investigar su comparabilidad. Los coeficientes de correlación de las dos pruebas son Y=101X-20.585y R=0,9844, respectivamente.
También te puede interesar: