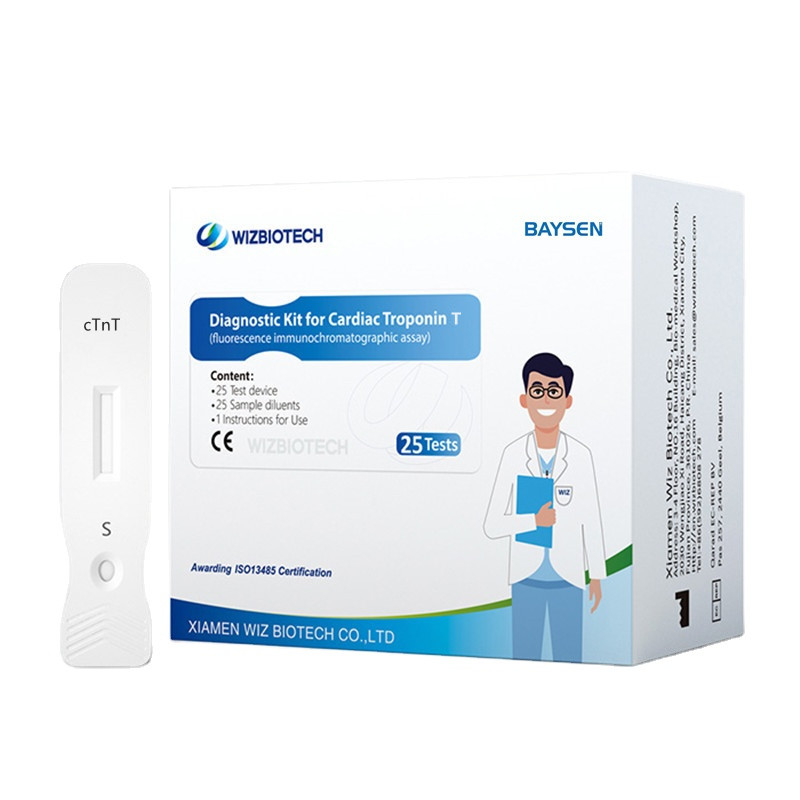
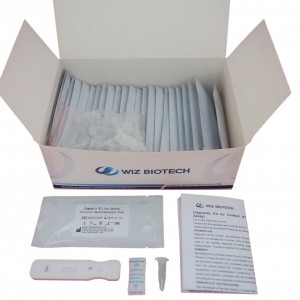
Kit de diagnóstico para la prueba rápida de troponina T cardíaca.
Kit de diagnóstico para troponina T cardíaca
Metodología: Ensayo inmunocromatográfico de fluorescencia
Información de producción
| Número de modelo | cTnT | Embalaje | 25 pruebas/kit, 30 kits/caja |
| Nombre | Kit de diagnóstico para troponina T cardíaca | Clasificación de instrumentos | Clase II |
| Características | Alta sensibilidad, fácil manejo. | Certificado | CE/ISO 13485 |
| Exactitud | > 99% | Duración | Dos años |
| Metodología | Ensayo inmunocromatográfico de fluorescencia | Servicio OEM/ODM | Disponible |
USO PREVISTO
Este kit está diseñado para la detección cuantitativa in vitro del contenido de troponina T cardíaca (cTnT) en muestras de suero, plasma o sangre total humana, y se utiliza como método auxiliar para el diagnóstico del infarto agudo de miocardio. Este kit solo proporciona el resultado de la prueba de troponina T cardíaca (cTnT), el cual debe analizarse junto con otra información clínica.
Procedimiento de prueba
| 1 | Antes de utilizar el reactivo, lea atentamente el prospecto y familiarícese con el procedimiento de uso. |
| 2 | Seleccione el modo de prueba estándar del analizador inmunológico portátil WIZ-A101. |
| 3 | Abra la bolsa de papel de aluminio que contiene el reactivo y saque el dispositivo de prueba. |
| 4 | Inserte el dispositivo de prueba horizontalmente en la ranura del analizador inmunológico. |
| 5 | En la página principal de la interfaz de funcionamiento del analizador inmunológico, haga clic en "Estándar" para acceder a la interfaz de prueba. |
| 6 | Haga clic en “Escaneo de control de calidad” para escanear el código QR que se encuentra en la parte interior del kit; introduzca los parámetros relacionados con el kit en el instrumento y seleccione el tipo de muestra. Nota: Cada número de lote del kit debe escanearse una sola vez. Si el número de lote ya se ha escaneado, omita este paso. |
| 7 | Compruebe que el "Nombre del producto", el "Número de lote", etc., en la interfaz de prueba coincidan con la información de la etiqueta del kit. |
| 8 | Retire el diluyente de la muestra una vez que la información sea consistente, agregue 80 μL de muestra de suero/plasma/sangre entera y mézclelos bien; |
| 9 | Agregue 80 µL de la solución previamente mezclada en el pocillo del dispositivo de prueba; |
| 10 | Una vez añadidas todas las muestras, haga clic en "Tiempo" y el tiempo de prueba restante se mostrará automáticamente en la interfaz. |
| 11 | El analizador inmunológico completará automáticamente la prueba y el análisis cuando se alcance el tiempo de prueba. |
| 12 | Una vez finalizada la prueba con el analizador inmunológico, el resultado se mostrará en la interfaz de prueba o podrá consultarse a través del "Historial" en la página principal de la interfaz de operación. |
Nota: cada muestra deberá ser pipeteada con una pipeta desechable limpia para evitar la contaminación cruzada.
Superioridad
Tiempo de prueba: 10-15 minutos
Almacenamiento: 2-30℃/36-86℉
Metodología: Ensayo inmunocromatográfico de fluorescencia
Característica:
• Alta sensibilidad
• Lectura del resultado en 15 minutos
• Fácil manejo
• 3 pruebas en una sola, ahorrando tiempo.
• Alta precisión

El desempeño clínico
El desempeño de la evaluación clínica del producto se evalúa mediante la recopilación de datos.150muestras clínicas. Utilice un kit ECLIA comercializado correspondiente como reactivo de control y compare los resultados de la prueba. Utilice regresión lineal para investigar su comparabilidad. Los coeficientes de correlación de las dos pruebas son Y=101X-20.585y R=0,9844, respectivamente.
También te puede interesar: