Pepsinogen I, Pepsinogen II und Gastrin-17 Kombi-Schnelltestkit
Diagnostik-Kit für Pepsinogen I/Pepsinogen II/Gastrin-17
Methodik: Fluoreszenz-Immunochromatographie-Test
Produktionsinformationen
| Modellnummer | G17/PGI/PGII | Verpackung | 25 Tests/Kit, 30 Kits/Karton |
| Name | Diagnostik-Kit für Pepsinogen I/Pepsinogen II/Gastrin-17 | Instrumentenklassifizierung | Klasse II |
| Merkmale | Hohe Empfindlichkeit, einfache Bedienung | Zertifikat | CE/ ISO13485 |
| Genauigkeit | > 99% | Haltbarkeit | Zwei Jahre |
| Methodik | Fluoreszenz-Immunochromatographie-Test | OEM/ODM-Service | Verfügbar |
VORGESEHENE VERWENDUNG
Dieses Kit eignet sich für den quantitativen In-vitro-Nachweis der Konzentration von Pepsinogen I (PGI) und Pepsinogen II.
(PGII) und Gastrin 17 in menschlichen Serum-/Plasma-/Vollblutproben zur Beurteilung der Magendrüsenzellen
Funktion, Magenfundusmukosaläsion und atrophische Gastritis. Das Kit liefert lediglich ein Testergebnis für Pepsinogen I.
(PGI), Pepsinogen II (PGII) und Gastrin 17. Das erhaltene Ergebnis wird in Kombination mit anderen klinischen Daten analysiert.
Diese Information darf nur von medizinischem Fachpersonal verwendet werden.
Testverfahren
| 1 | Lesen Sie vor der Verwendung des Reagenz die Packungsbeilage sorgfältig durch und machen Sie sich mit den Arbeitsanweisungen vertraut. |
| 2 | Wählen Sie den Standardtestmodus des tragbaren Immunanalysators WIZ-A101. |
| 3 | Öffnen Sie die Aluminiumfolienverpackung des Reagenz und entnehmen Sie das Testgerät. |
| 4 | Das Testgerät wird horizontal in den Schlitz des Immunanalysators eingeführt. |
| 5 | Klicken Sie auf der Startseite der Bedienoberfläche des Immunanalysators auf „Standard“, um zur Testschnittstelle zu gelangen. |
| 6 | Klicken Sie auf „QC Scan“, um den QR-Code auf der Innenseite des Kits zu scannen; geben Sie die kitbezogenen Parameter in das Gerät ein und Probentyp auswählen. Hinweis: Jede Chargennummer des Kits muss einmal gescannt werden. Wenn die Chargennummer bereits gescannt wurde, dann Diesen Schritt überspringen. |
| 7 | Prüfen Sie, ob die Angaben zu „Produktname“, „Chargennummer“ usw. auf der Testoberfläche mit den Informationen auf dem Kit übereinstimmen. Etikett. |
| 8 | Nachdem die Konsistenz der Informationen bestätigt wurde, entfernen Sie die Probenverdünnungsmittel und geben Sie 80 µL Serum/Plasma/Vollblut hinzu. Probe nehmen und ausreichend vermischen. |
| 9 | Geben Sie 80µL der oben gemischten Lösung in die Probenöffnung des Testgeräts. |
| 10 | Nachdem die gesamte Probe hinzugefügt wurde, klicken Sie auf „Zeitmessung“. Die verbleibende Testzeit wird automatisch angezeigt. Schnittstelle. |
| 11 | Das Immunanalysegerät führt Test und Analyse automatisch durch, sobald die Testzeit erreicht ist. |
| 12 | Ergebnisberechnung und -anzeige Nach Abschluss des Tests mit dem Immunanalysator wird das Testergebnis auf der Testoberfläche angezeigt oder kann eingesehen werden. über „Verlauf“ auf der Startseite der Bedienoberfläche. |
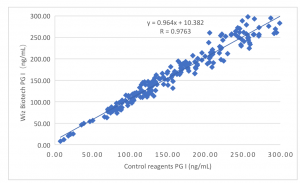
Die klinische Leistung
Die klinische Leistungsfähigkeit des Produkts wird anhand von 200 klinischen Proben bewertet. Als Kontrollreagenz wird ein handelsüblicher ELISA-Test verwendet. Die Ergebnisse des PGI-Tests werden verglichen. Die Vergleichbarkeit wird mittels linearer Regression untersucht. Die Korrelationskoeffizienten der beiden Tests betragen y = 0,964X + 10,382 bzw. R = 0,9763. Die Ergebnisse des PGII-Tests werden verglichen. Die Vergleichbarkeit wird mittels linearer Regression untersucht. Die Korrelationskoeffizienten der beiden Tests betragen y = 1,002X + 0,025 bzw. R = 0,9848. Die Ergebnisse des G-17-Tests werden verglichen. Die Vergleichbarkeit wird mittels linearer Regression untersucht. Die Korrelationskoeffizienten der beiden Tests betragen y = 0,983X + 0,079 bzw. R = 0,9864.
Das könnte Ihnen auch gefallen: