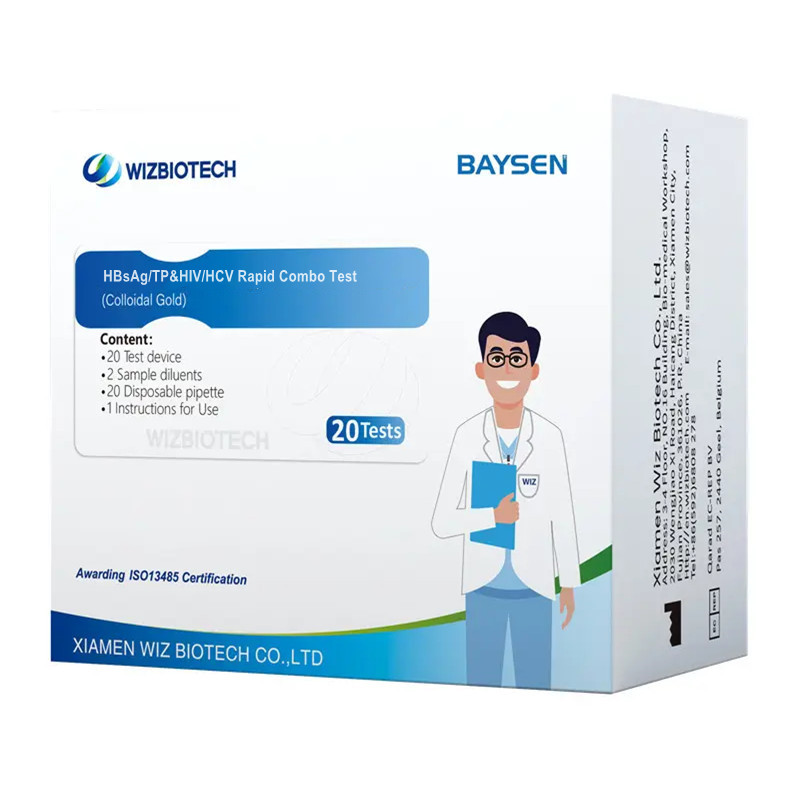
Schnelltest auf infektiöses HIV, HCV, HBsAg und Syphilis
PRODUKTIONSINFORMATIONEN
| Modellnummer | HBsAg/TP&HIV/HCV | Verpackung | 20 Tests/Kit, 30 Kits/Karton |
| Name | HBsAg/TP&HIV/HCV Schnelltest | Instrumentenklassifizierung | Klasse III |
| Merkmale | Hohe Empfindlichkeit, einfache Bedienung | Zertifikat | CE/ ISO13485 |
| Genauigkeit | > 97% | Haltbarkeit | Zwei Jahre |
| Methodik | Kolloidales Gold | OEM/ODM-Service | Verfügbar |
Überlegenheit
Testdauer: 15-20 Minuten
Lagerung: 2-30℃/36-86℉
Methodik: Kolloidales Gold
Besonderheit:
• Hochsensibel
• Ergebnisablesung in 15-20 Minuten
• Einfache Bedienung
• Hohe Genauigkeit
VORGESEHENE VERWENDUNG
Dieses Kit eignet sich für die qualitative In-vitro-Bestimmung von Hepatitis-B-Virus, Syphilis-Spirochäte, humanem Immunschwächevirus und Hepatitis-C-Virus in menschlichem Serum/Plasma.ma/Vollblutproben zur ergänzenden Diagnostik von Hepatitis-B-Virus-, Syphilis-Spirochäten-, HIV- und Hepatitis-C-Virus-Infektionen. Die erzielten Ergebnisse solltenDie Daten müssen in Verbindung mit anderen klinischen Informationen analysiert werden. Sie sind ausschließlich für die Verwendung durch medizinisches Fachpersonal bestimmt.
Testverfahren
| 1 | Lesen Sie die Gebrauchsanweisung sorgfältig durch und befolgen Sie die Anweisungen genau, um die Genauigkeit der Testergebnisse nicht zu beeinträchtigen. |
| 2 | Vor dem Test werden das Testkit und die Probe aus dem Lager genommen, auf Raumtemperatur gebracht und entsprechend gekennzeichnet. |
| 3 | Die Verpackung des Aluminiumfolienbeutels aufreißen, das Testgerät herausnehmen, es markieren und anschließend waagerecht auf den Testtisch legen. |
| 4 | Serum-/Plasmaproben mit einer Einwegpipette aspirieren und jeweils 2 Tropfen in die Vertiefungen s1 und s2 geben; bei Vollblutproben jeweils 3 Tropfen in die Vertiefungen s1 und s2 geben, bevor 1–2 Tropfen Spüllösung in jede Vertiefung s1 und s2 gegeben werden und die Zeitmessung startet. |
| 5 | Die Testergebnisse sollten innerhalb von 15 bis 20 Minuten interpretiert werden; nach mehr als 20 Minuten interpretierte Ergebnisse sind ungültig. |
| 6 | Die visuelle Interpretation kann zur Ergebnisinterpretation herangezogen werden. |
Hinweis: Jede Probe muss mit einer sauberen Einwegpipette pipettiert werden, um Kreuzkontaminationen zu vermeiden.
KLINISCHE LEISTUNG
| WIZ-ErgebnisseHBsag
| Testergebnis des Referenzreagenz | Positive Übereinstimmungsrate: 99,06 % (95%-KI 96,64%~99,74%) Negative Übereinstimmungsrate: 98,69 % (95%-KI 96,68%~99,49%) Gesamtübereinstimmungsrate: 98,84 % (95%-KI 97,50%~99,47%) | ||
| Positiv | Negativ | Gesamt | ||
| Positiv | 211 | 4 | 215 | |
| Negativ | 2 | 301 | 303 | |
| Gesamt | 213 | 305 | 518 | |
| WIZ-ErgebnisseTP
| Testergebnis des Referenzreagenz | Positive Übereinstimmungsrate: 96,18 % (95%-KI 91,38%~98,36%) Negative Übereinstimmungsrate: 97,67 % (95%-KI 95,64%~98,77%) Gesamtübereinstimmungsrate: 97,30 % (95%-KI 95,51%~98,38%) | ||
| Positiv | Negativ | Gesamt | ||
| Positiv | 126 | 9 | 135 | |
| Negativ | 5 | 378 | 383 | |
| Gesamt | 131 | 387 | 518 | |
| WIZ-ErgebnisseHCV
| Testergebnis des Referenzreagenz | Positive Übereinstimmungsrate: 93,44 % (95%-KI 84,32%~97,42%) Negative Übereinstimmungsrate: 99,56 % (95%-KI 98,42%~99,88%) Gesamtübereinstimmungsrate: 98,84 % (95%-KI 97,50%~99,47%) | ||
| Positiv | Negativ | Gesamt | ||
| Positiv | 57 | 2 | 59 | |
| Negativ | 4 | 455 | 459 | |
| Gesamt | 61 | 457 | 518 | |
| WIZ-ErgebnisseHIV
| Testergebnis des Referenzreagenz | Positive Übereinstimmungsrate: 96,81 % (95%-KI 91,03%~98,91%) Negative Übereinstimmungsrate: 99,76 % (95%-KI 98,68%~99,96%) Gesamtübereinstimmungsrate: 99,23 % (95%-KI 98,03%~99,70%) | ||
| Positiv | Negativ | Gesamt | ||
| Positiv | 91 | 1 | 92 | |
| Negativ | 3 | 423 | 446 | |
| Gesamt | 94 | 424 | 518 | |